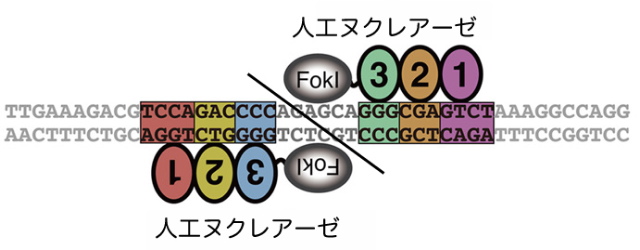
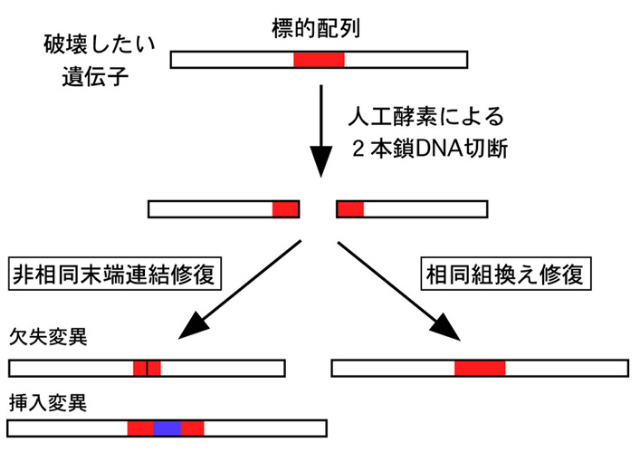
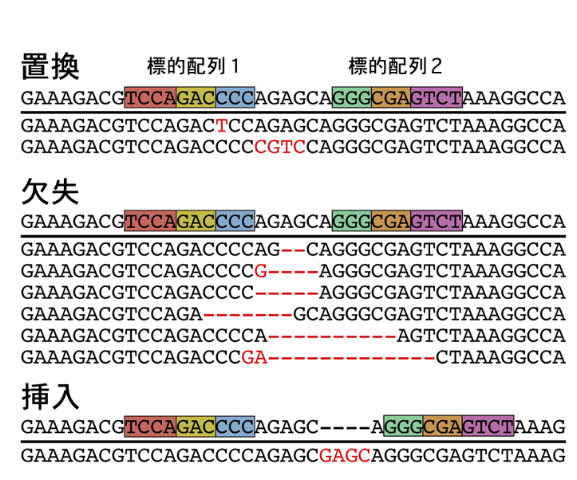
近年、様々な生物種において標的遺伝子を改変する技術として、人工ヌクレアーゼ(ZFNやTALEN)を利用した“ゲノム編集”が注目されている。人工ヌクレアーゼは、DNAに特異的に結合するドメインと、制限酵素FokIのDNA切断ドメインを連結させたキメラタンパク質である。2つの人工ヌクレアーゼが近接する標的配列に結合するとDNA切断ドメインが2量体となりDNAを切断する。切断されたDNAは、相同組換えあるいは非相同末端連結により修復されるが、この時に目的の遺伝子を改変することが可能となる。標的配列の選択が可能であることから次世代のノックアウト技術として注目され、様々な動物、植物、哺乳類培養細胞(ES細胞やiPS細胞を含む)において成功例が報告されている。人工ヌクレアーゼに加えて、2013年始めに細菌や古細菌の獲得免疫系を利用したCRISPR/Cas9システムが報告され、今後はCRISPR/Casが中心的なツールとして利用されると予想される。
我々は、オープンリソースを利用した人工ヌクレアーゼの作製方法を確立し、ウニ胚をモデルとしてZinc finger nucleases (ZFNs)による遺伝子破壊(Ochiai et al., 2010)およびレポーター遺伝子のノックインを行ってきた(Ochiai et al., 2012)。加えて、植物細菌Xanthomonas由来のTranscription activator like effector(TALE)のDNA結合ドメインを利用したTALE nucleases (TALENs)による遺伝改変技術を確立し(Sakuma et al., 2013)、様々な生物(ラット、マウス、マーモセット、ホヤ、ウニ、ショウジョウバエ、コオロギ、ウニ、植物)での標的遺伝子の改変を進めてきた。さらに、CRISPR/Cas9のマルチガイドシステムを確立し、培養細胞における複数同時改変が可能なことを証明した(Sakuma et al., 2014)。
Ochiai et al., Targeted mutagenesis in the sea urchin embryo using zinc-finger nucleases, Genes to Cells, 15:875-885 (2010)
Ochiai et al., Zinc-finger nuclease-mediated targeted insertion of reporter genes for quantitative imaging of gene expression in sea urchin embryos, Proc Natl Acad Sci U S A, 109: 10915-10920 (2012)
Sakuma et al., Efficient TALEN construction and evaluation methods for human cell and animal applications, Genes to Cells, 18: 315-326 (2013)
Sakuma et al., Multiplex genome engineering in human cells using all-in-one CRISPR/Cas9 vector system, Scientific Reports, 4: 5400 (2014)
 研究内容へ戻る
研究内容へ戻る












